上海细胞库
人源细胞系| 稳转细胞系| 基因敲除株| 基因点突变细胞株| 基因过表达细胞株| 重组细胞系| 猪的细胞系| 马细胞系| 兔的细胞系| 犬的细胞系| 山羊的细胞系| 鱼的细胞系| 猴的细胞系| 仓鼠的细胞系| 狗的细胞系| 牛的细胞| 大鼠细胞系| 小鼠细胞系| 其他细胞系|
| 规格 | 价格 | 库存 |
|---|---|---|
| 200-1000次 | ¥ 980 | 200 |
本试剂盒提供了染色增强剂,使细胞膜染色更加快速,荧光染色更加明亮,染色背景更低。
本试剂盒除了最简单的细胞膜荧光标记外,还可以用于检测细胞的融合和粘附,检测发育或移植过程中细胞迁移,通过FRAP (Fluorescence Recovery After Photobleaching)检测脂在细胞膜上的扩散,检测细胞毒性和标记脂蛋白等。
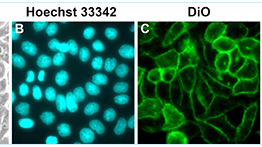
本试剂盒可以直接染色活的细胞或组织,染色时间通常为5-20分钟。对于固定的细胞或组织,通常宜使用配制在PBS中的4%多聚甲醛进行固定,使用其它不适当的固定液会导致荧光背景较高。本试剂盒对HeLa细胞的染色效果参考图2。
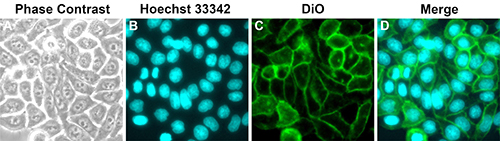
图2. 细胞膜绿色荧光染色试剂盒(DiO)对HeLa细胞的染色效果。DiO的染色时间为10分钟。
DiO染色后可以兼容免疫荧光实验。建议使用免疫染色通透液(Saponin) (P0095)或使用洋地黄皂苷(ST1272)配制的不会溶解细胞膜的通透液进行通透,其它去垢剂配制的通透液可能会溶解细胞膜上的脂类物质,造成DiO失去结合位置,最终导致DiO的染色失效。但通透也可能会影响DiO在细胞膜上的定位并会增加细胞内的染色,具体实验中需根据实验的需求选择合适的细胞通透液。
本试剂盒小包装C1993S,如果用于流式细胞仪,每个样品的检测体系体积为0.5ml时,可以进行200次检测;96孔板每孔检测体系的体积为100μl时可以进行1000次检测。
包装清单:
| 产品编号 | 产品名称 | 包装 |
| C1993S-1 | DiO (400X) | 0.25ml |
| C1993S-2 | 染色增强剂(400X) | 0.25ml |
| C1993S-3 | 染色缓冲液 | 100ml |
| — | 说明书 | 1份 |
保存条件:
-20℃避光保存,一年有效。染色增强剂(400X)和染色缓冲液也可保存在4℃。
注意事项:
荧光染料均存在淬灭问题,请尽量注意避光,以减缓荧光淬灭。
染色缓冲液经过过滤除菌处理,在使用时须注意避免微生物污染,否则很可能严重影响染色效果。如果染色缓冲液发生浑浊等明显的微生物污染,就不能继续使用。
如果染色时间过长或染色后细胞继续培养,探针也可能进入细胞内而染色其它细胞器的膜。
本产品仅限于专业人员的科学研究用,不得用于临床诊断或治疗,不得用于食品或药品,不得存放于普通住宅内。
为了您的安全和健康,请穿实验服并戴一次性手套操作。
使用说明:
1.溶液制备:
a.细胞膜染色工作液的用量:对于6、12、24、96孔板,每孔的细胞膜染色工作液分别为1~2ml、0.5~1ml、300~500μl和50~100μl;对于流式细胞样品,每个样品的细胞膜染色工作液为0.5ml;对于切片,可以根据切片大小,每个切片使用100-200μl的细胞膜染色工作液。
b.细胞膜染色工作液的配制:根据样品数量和每个样品所需工作液的体积,计算出细胞膜染色工作液的总体积。以流式细胞仪检测为例,每个样品的细胞膜染色工作液为0.5ml,参照下表配制细胞膜染色工作液。
注意:请严格按照下表中组分顺序和体积配制细胞膜染色工作液,且DiO (400X)和染色增强剂(400X)混匀后再加入染色缓冲液。对于活细胞染色的情况,如果细胞对于培养条件非常敏感,也可以使用正常的细胞培养液代替本试剂盒提供的染色缓冲液用于配制细胞膜染色工作液。使用正常的细胞培养液替代染色缓冲液的情况,可能会导致染色效果有所下降,此时需要适当考虑延长染色时间或加大DiO染料浓度。
| 样品数 | 2 | 20 | 200 |
| DiO (400X) | 2.5μl | 25μl | 250μl |
| 染色增强剂(400X) | 2.5μl | 25μl | 250μl |
| 染色缓冲液 | 995μl | 9.95ml | 99.5ml |
| 细胞膜染色工作液总体积 | 1ml | 10ml | 100ml |
注:不同细胞的最佳染色浓度略有不同,细胞膜染色工作液的最终浓度建议根据不同细胞系和实验体系进行优化,可在1:100-1:400之间进行调整。DiO的最终浓度提高时,染色增强剂的用量不变。
2.悬浮活细胞染色:
a.加入适当体积的细胞膜染色工作液重悬细胞,使其密度为1-2×106/ml左右。
b.37℃避光孵育细胞5-20min,不同的细胞最佳孵育时间不同。以5min作为初始孵育时间,根据实际所用的细胞优化染色时间,以得到最佳的荧光染色效果。
c.500-1000×g室温离心5min。
d.吸除上清液,再次缓慢加入37℃预热的细胞培养液重悬细胞。
e.重复c、d步骤两次。
f.流式细胞仪检测,或将细胞转移至多孔板、细胞培养皿或者细胞爬片上,在荧光显微镜下观察。DiO的最大激发光波长为484nm,最大发射光波长为501nm。
3.贴壁活细胞染色:
a.将贴壁细胞种于细胞培养皿、多孔细胞培养板或者细胞爬片上。
b.吸除细胞培养液,用Hanks' Balanced Salt Solution (C0218或C0219)或PBS (C0221A、C0221D或C0221G)洗涤细胞2遍。
c.加入适当体积的细胞膜染色工作液,轻轻晃动使染料均匀覆盖所有细胞。
d.37℃避光孵育细胞5-20min,不同的细胞最佳培养时间不同。以5min作为初始孵育时间,根据实际所用的细胞优化染色时间,以得到最佳的荧光染色效果。
e.吸除细胞膜染色工作液,用Hanks' Balanced Salt Solution或PBS洗涤2-3次,然后加入37℃预热的细胞培养液即可在荧光显微镜下观察。DiO的最大激发光波长为484nm,最大发射光波长为501nm。
4.染色后的固定和通透:
a.固定:如果样品需要进一步进行免疫荧光实验,建议使用免疫染色固定液(P0098)或4%多聚甲醛固定液(P0099)进行固定。
b.通透:建议使用0.1% Triton X-100 (ST795)或洋地黄皂苷(ST1272)进行通透。但通透可能会影响DiO在细胞膜的定位并会增加细胞内的染色,具体实验中需根据实验的需求选择合适的细胞通透液。
注:如果需要封片,建议直接用PBS进行封片。请避免使用含有甘油或其它有机物的封片剂,否则会影响染色并增加荧光背景。
5.固定后细胞或切片的染色:
a.使用4%多聚甲醛固定液(P0099)或免疫染色固定液(P0098)进行固定。
b.吸除固定液,用PBS洗涤细胞3遍。
c.选做:使用配制在PBS中的0.1% Triton X-100 (ST795)进行通透,室温10min。然后用PBS洗涤细胞3遍。
d.选做:按照免疫染色的方法进行抗体的孵育或用其它染料进行染色。注意:抗体孵育步骤中的封闭液、抗体稀释液及洗涤液不能含有去垢剂。
e.加入适当体积的细胞膜染色工作液,轻轻晃动使染料均匀覆盖所有细胞或样品。
f.37℃避光孵育5-20min,最佳染色时间需要根据自己的实验条件摸索,以达到最佳的荧光染色效果。
g.吸除细胞膜染色工作液,用PBS洗涤2-3次,随后即可在荧光显微镜下观察。DiO的最大激发光波长为484nm,最大发射光波长为501nm。